 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知298K时下列两个反应的平衡常数: 试求反应在该温度下的平衡常数。
已知298K时下列两个反应的平衡常数:
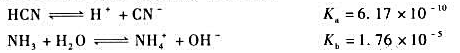
试求反应 在该温度下的平衡常数。
在该温度下的平衡常数。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298K时下列两个反应的平衡常数:
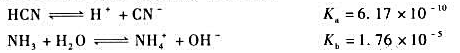
试求反应 在该温度下的平衡常数。
在该温度下的平衡常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知298K时下列两个反应的平衡常数: 试求反应在该温度下的…”相关的问题
更多“已知298K时下列两个反应的平衡常数: 试求反应在该温度下的…”相关的问题
将下列氧化还原反应设计成为两个半电池反应,并利用标准电极电势表的数据,求出298K时反应的平衡常数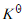 。
。
已知298K时,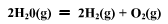 反应的平衡常数为9.7×10-81,这时H2O(1)的饱和蒸气压为3200Pa,试求298K时下述电池的电动势E。
反应的平衡常数为9.7×10-81,这时H2O(1)的饱和蒸气压为3200Pa,试求298K时下述电池的电动势E。
Pt|H2(P3)|H2SO4(0.01mol·kg-1)|O2(P3)|Pt
(298K时的平衡常数是根据高温下的数据间接求出的。由于氧电极上反应不易达到平衡,不能测出E的精确值,所以可通过此法来计算E值。)
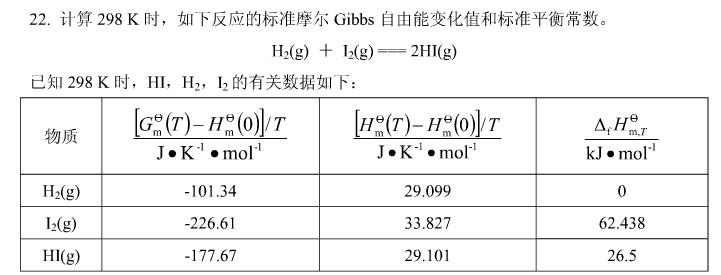
计算298K时,如下反应的标准摩尔Gibbs自由能变化值和标准平衡常数。
H2(g)+I2(g)====2HI(g)
已知298K时,HI、H2、I2的有关数据如下:
已知反应:
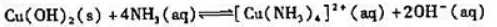
(1)计算该反应在298K下的标准平衡常数;
(2)估算Cu(OH)2在6.0mol·L-1氨水中的溶解度(mol·L-1)(忽略氨水浓度的变化).