 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,将饱和甘汞电极与标准锌电极组成一个原电池,则该原电池的电池符号是()原电池的正极反
25℃时,将饱和甘汞电极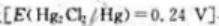
与标准锌电极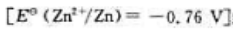 组成一个原电池,则该原电池的电池符号是()原电池的正极反应为
组成一个原电池,则该原电池的电池符号是()原电池的正极反应为
().负极反应为(),电池反应为()。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,将饱和甘汞电极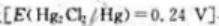
与标准锌电极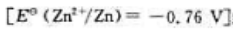 组成一个原电池,则该原电池的电池符号是()原电池的正极反应为
组成一个原电池,则该原电池的电池符号是()原电池的正极反应为
().负极反应为(),电池反应为()。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“25℃时,将饱和甘汞电极与标准锌电极组成一个原电池,则该原电…”相关的问题
更多“25℃时,将饱和甘汞电极与标准锌电极组成一个原电池,则该原电…”相关的问题
将标准Ag-AgCl电极Eθ(AgCl/Ag)=0.2222V与饱和甘汞电极Eθ=0.2145V组成原电池,该原电池的电池符号______;正极反应______;负极反应______;电池反应______;电池反应的平衡常数______。
将Ag---AgCl电极[E(AgCl/Ag)=0.2222V]与饱和甘汞电极[E=0.2415v]组成原电池, 该原电池的电池符号为________________;正极反应________________;负极反应______________;电池反应___________________;电池的平衡常数为________________.
将Ag—AgCl电极[Eθ(AgCl/Ag)=0.2222V)]与饱和甘汞电极[Eθ=0.2415V]组成原电池,该原电池的电池符号为______;正极反应______;负极反应______;电池反应______;电池反应的平衡常数为______。
写出标准锌电极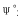 (Zn[2+/Zn)=-0.763V]与甘汞电极(
(Zn[2+/Zn)=-0.763V]与甘汞电极(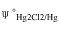 =0.2415V)组成的原电池符号是______,其中正极反应是______,负极反应是______,电池反应是______,平衡常数为______。
=0.2415V)组成的原电池符号是______,其中正极反应是______,负极反应是______,电池反应是______,平衡常数为______。
写出标准锌电极[Eθ(Zn2+/Zn)=一0.763 V]与甘汞电极(Eθ=0.2415 V)组成的原电池符号是________________________________________________,其中正极反应是________________________________________________,负极反应是________________________________,电池反应是________________________________,平衡常数为________________。
将反应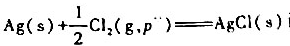 设计成原电池.已知25°C;时,
设计成原电池.已知25°C;时,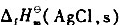 =-127.07kJ.mol-1.
=-127.07kJ.mol-1.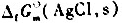 =-109.79kJ.mol-1,标准电极电势
=-109.79kJ.mol-1,标准电极电势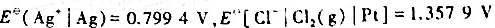 .
.
(1)写出电极反应和电池图示;
(2)求25°C、电池可逆放电2F电荷悬时的热Qz;
(3)求25°C时AgCl的活度积Kap.
5.写出下列原电池的电极反应式和电池反应式,并计算25℃时原电池的电动势。
Fe|Fe2+(1.0mol/L)||Cl-(1.0mol/L)|Cl2(100kpa),Pt
将下列反应组成原电池(温度为298.15K):2Fe3++Cu====2Fe2++Cu2+
(1)计算原电池的标准电动势;(2)写出其电池符号;(3)指出正极、负极,并写出电极反应;(4)当Cu2+的浓度升到10mol·L-1时,原电池的电动势为多少?
将—ClO4—选择性电极插入50.00mL某高氯酸盐待测溶液,与饱和甘汞电极(为负极)组成原电池,测得电动势为358.7mV;将待测溶液换成0.0300mol.L—1标准溶液后,测得电动势为346.1mV,求待测溶液中ClO4—浓度。