 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算25℃,100kPa下反应CaCO3(s)→CaO(s)+CO2(g)的景和,并判断: (1)上述反应能否自发进行? (2)对上述反应,是

查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算25℃,100kPa下反应CaCO3(s)→CaO(s)…”相关的问题
更多“计算25℃,100kPa下反应CaCO3(s)→CaO(s)…”相关的问题
实验室里,常用下面的反应制备氯气。
MnO2+4HCl→MnCl2+Cl2+2H2O
(1)根据标准电极电势判断,上述反应在标准状态时能否自发进行?
(2)假如用浓盐酸(12.0mol·L-1),上述反应能否自发进行?(令p(Cl2)=100kPa,c(Mn2+)=1.00mol·L-1)
利用热力学数据计算5题中反应在298.15K时的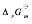 ,并判断在标准状态下该反应能否自发进行?
,并判断在标准状态下该反应能否自发进行?

写出下列各电池的电池反应。应用表7.7.1(在教材中)的数据计算25℃时各电池的电动势及电池反应的摩尔吉布斯函数变,并指明各电池反应能否自发进行。
(1)Pt|H2(g,100kPa)|HCl[a(HCl)=1]|Cl2(g,100kPa)|Pt
(2)Zn|ZnCl2[a(ZnCl2)=0.5]|AgCl(S)|Ag
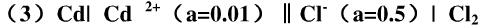
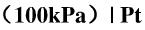
制备半导体材料时发生如下反应,并已知相应热力学数据:
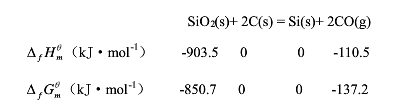
通过计算回答下列问题:
(1)标态下,398.15K时,反应能否自发进行
(2)标态下,反应自发进行的温度
写出下列电池的电池反应:
Cd(s)|Cd2+(a=0.01)|Cl-(a=0.5)|Cl2(100kPa)|Pt,并计算298K时,各电极的电极电势及电池电动势,根据计算结果指出此电池反应能否自发进行?
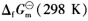 是902.9 kJ.mol-1,计算下述光合作用反应的
是902.9 kJ.mol-1,计算下述光合作用反应的
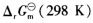 ,并判断这个反应能否自发进行。 6CO2(g)+6HO2(1)
,并判断这个反应能否自发进行。 6CO2(g)+6HO2(1)
 C6H12O6(s)+6O2(g)
C6H12O6(s)+6O2(g)
NH4Cl(s)====NH3(g)+HCl(g)
在25℃下,下有: