 更多“在利用最简公式求算一元弱酸HA溶液中H3O+浓度时,除了要求…”相关的问题
更多“在利用最简公式求算一元弱酸HA溶液中H3O+浓度时,除了要求…”相关的问题
第1题
使用最简式计算元弱酸HA溶液中,H3O+浓度,需要满足的两个条件是()和()。
使用最简式计算元弱酸HA溶液中,H3O+浓度,需要满足的两个条件是()和()。
点击查看答案
使用最简式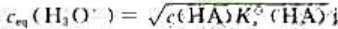 计算元弱酸HA溶液中,H3O+浓度,需要满足的两个条件是()和()。
计算元弱酸HA溶液中,H3O+浓度,需要满足的两个条件是()和()。
第2题
计算一元弱酸溶液的c(H+),常用的最简式为c(H+)=______,使用此式时要先检查是否满足两个条件:______和______
计算一元弱酸溶液的c(H+),常用的最简式为c(H+)=______,使用此式时要先检查是否满足两个条件:______和______,否则将引入较大误差。
第3题
将0.050dm3,浓度为0.10mol·dm-3一元弱酸HA溶液与0.020dm3,0.10mol·dm-3KOH溶液混合后稀释至0.10dm3,测得溶
将0.050dm3,浓度为0.10mol·dm-3一元弱酸HA溶液与0.020dm3,0.10mol·dm-3KOH溶液混合后稀释至0.10dm3,测得溶液pH=5.25,求HA的解离常数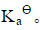 。
。
第6题
今有一元弱酸HA在0.10mol·L-1溶液中有2.0%解离。试计算: (1)HA的Ka; (2)在0.050mol·L-1溶液中的解离度;
今有一元弱酸HA在0.10mol·L-1溶液中有2.0%解离。试计算:
(1)HA的Ka;
(2)在0.050mol·L-1溶液中的解离度;
(3)溶液浓度为多少时有1.0%的解离?
第7题
某一元弱酸HA的浓度为0.010mol·L-1,在常温下测得其pH为4.0。求该一元弱酸的解离平衡常数和解离度。
某一元弱酸HA的浓度为0.010mol·L-1,在常温下测得其pH为4.0。求该一元弱酸的解离平衡常数和解离度。
第8题
某一元弱酸HA溶液的[H+]=amol•dm-3,在此溶液中加入过量难溶盐MA,实现沉淀溶解平衡时,溶液的[H+
某一元弱酸HA溶液的[H+]=amol•dm-3,在此溶液中加入过量难溶盐MA,实现沉淀溶解平衡时,溶液的[H+]=bmol•dm-3。设酸的浓度满足解离平衡的近似计算条件,求MA的溶度积常数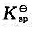 。
。
第9题
计算一元弱碱溶液的c(OH-)值,常用的最简式为c(OH-)=______,使用此式时应先满足两个条件,即______和______。
计算一元弱碱溶液的c(OH-)值,常用的最简式为c(OH-)=______,使用此式时应先满足两个条件,即______和______。
第10题
对一元弱酸HA,当{c}/Ka=500时: (1)比较H+浓度的最简计算式和近似计算式(忽略水的解离)两者的计算误差;
对一元弱酸HA,当{c}/Ka=500时:
(1)比较H+浓度的最简计算式

(2)计算HAc(Ka=1.76×10-5)在两种情况下的解离度的差值;
(3)解释在用最简式计算时,{c)/Ka=500的意义。


 如果结果不匹配,请
如果结果不匹配,请 
















