 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知反应2SO2(g)+O2(g)2SO3(g)在427℃和527℃时的KΘ值分别为1.0×105和1.1×102,求该反应的。

查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应2SO2(g)+O2(g)2SO3(g)在427℃和…”相关的问题
更多“已知反应2SO2(g)+O2(g)2SO3(g)在427℃和…”相关的问题
已知在427℃时各物质的热力学函数
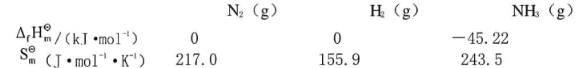 在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[H2]=3.0mol·dm-3。求NH3的浓度。
在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[H2]=3.0mol·dm-3。求NH3的浓度。
已知液态松节油萜的消旋作用是一级反应,在458K和510K时速率常数分别为k(458K)=2.2×10-5min-1和k(510K)=3.07×10-3min-1。试求反应的实验活化能Ea,以及在平均温度时的活化焓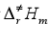 、活化熵
、活化熵 和活化Gibbs自由能
和活化Gibbs自由能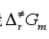 。
。
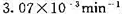 。试求反应的实验活化能
。试求反应的实验活化能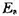 ,以及在平均温度时的活化焓
,以及在平均温度时的活化焓
 308 K时,
308 K时,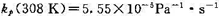 .若A(g)和B(g)的原子半径和摩尔质量分别为
.若A(g)和B(g)的原子半径和摩尔质量分别为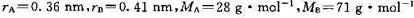 .试求在298 K时,(1)该反应的概率因子P;(2)反应的活化焓
.试求在298 K时,(1)该反应的概率因子P;(2)反应的活化焓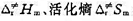 和活化Gibbs自由能
和活化Gibbs自由能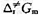 .
.
已知反应: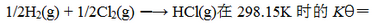
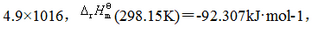 ,求在500K时的
,求在500K时的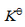 值[近似计算,不查
值[近似计算,不查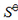 (298.15K)和
(298.15K)和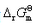 (298.15K)数据]。
(298.15K)数据]。
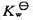 在293 K和303K时分别为
在293 K和303K时分别为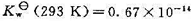 和
和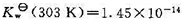 .试求:(1) 298 K和标准压力时,中和反应
.试求:(1) 298 K和标准压力时,中和反应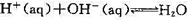 (1)的
(1)的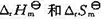 的值(设
的值(设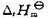 与温度的关系可以忽略);(2) 298 K时OH-的标准摩尔生成Gibbs 自由能
与温度的关系可以忽略);(2) 298 K时OH-的标准摩尔生成Gibbs 自由能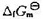 的值。
的值。已知下述电池的标准电动势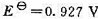 :
:
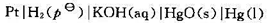
并已知反应 .
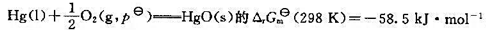
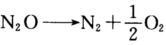 的速率常数k=0.1 35 s-1,在1 085 K时k=3.70 s-1,求此反应的活化能Ea。
的速率常数k=0.1 35 s-1,在1 085 K时k=3.70 s-1,求此反应的活化能Ea。
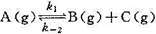 ,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298 K升到310 K时,k和k-2的值均增加1倍,试求:
,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298 K升到310 K时,k和k-2的值均增加1倍,试求:(1)298K时的反应平衡常数Kp;
(2)正、逆反应的实验活化能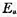 ;
;
(3)298K时反应的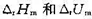 ;
;
(4)在298K时,A的起始压力为100kPa,若使总压力达到152kPa,所需的时间。